Intermolekylære bindinger er de bindinger, der holder molekyler sammen. Disse bindinger er ofte svagere end intramolekylære bindinger, som er de bindinger, der holder atomer sammen i et molekyle.
Der findes flere forskellige typer af intermolekylære bindinger, og deres styrke varierer betydeligt. Nogle intermolekylære bindinger er så svage, at de kan brydes ved relativt lave temperaturer, mens andre er så stærke, at de kan modstå høje temperaturer og store mekaniske belastninger.
Typer af intermolekylære bindinger
Der findes mange forskellige typer af intermolekylære bindinger, og de kan deles op i følgende kategorier:
London-kræfter
London-kræfter, er de svage, elektrostatiske kræfter, der opstår mellem alle typer af atomer og molekyler. Disse kræfter opstår, når elektroner i et molekyle bevæger sig, hvilket resulterer i en midlertidig ujævn fordeling af elektronerne. Denne ujævne fordeling af elektroner resulterer i en midlertidig polarisering af molekylet, hvilket igen resulterer i en attraktion mellem molekylerne.
London-kræfter er de svagere intermolekylære bindinger, og deres styrke stiger med størrelsen af molekylerne.
Dipol-dipol interaktioner
Dipol-dipol interaktioner er de elektrostatiske kræfter, der opstår mellem permanente dipoler i molekyler. En permanent dipol er en ujævn fordeling af elektroner i et molekyle, hvilket resulterer i en positiv ladning på den ene ende af molekylet og en negativ ladning på den anden ende. Når to molekyler med permanente dipoler er tæt på hinanden, vil de positive og negative ender tiltrække hinanden, hvilket resulterer i en attraktion mellem molekylerne. Dipol-dipol interaktioner er stærkere end dispersion forces, men stadig relativt svage sammenlignet med andre typer af intermolekylære bindinger.
Ion-dipol interaktioner
Ion-dipol interaktioner er en type intermolekylær binding, der opstår mellem ioner og polariserede molekyler.
Når et ion – enten positivt ladet eller negativt ladet – kommer tæt på et polariseret molekyle, vil de elektriske ladninger i ionet og polariseringen i molekylet tiltrække hinanden. Dette resulterer i en attraktion mellem ionet og molekylet, hvilket kaldes for en ion-dipol interaktion.
Ion-dipol interaktioner er stærkere end de svagere intermolekylære bindinger, londonkræfter og dipol-dipol interaktioner, men stadig svagere end de stærkere ion-ion interaktioner og hydrogenbånd.
Styrken af ion-dipol interaktioner afhænger af ladningen på ionet og polariseringen af molekylet, så jo stærkere ladningen på ionet og polariseringen af molekylet er, jo stærkere vil ion-dipol interaktionen være.
Ion-dipol interaktioner findes i mange molekyler, herunder vand og andre vandopløselige stoffer. Disse molekyler opløses let i vand på grund af de stærke ion-dipol interaktioner mellem vandmolekylerne og de opløste stoffer. Ion-dipol interaktioner spiller også en vigtig rolle i mange kemiske reaktioner, da de kan påvirke stabiliteten og reaktiviteten af de involverede molekyler.
I termodynamisk sammenhæng kan ion-dipol interaktioner beskrives ved hjælp af entalpi. Når ion-dipol interaktioner brydes, vil dette medføre en entalpifrigørelse, hvilket kan måles ved hjælp af et Kalorimeter. Ved at måle entalpifrigørelsen ved brud på ion-dipol interaktioner kan man beregne styrken af ion-dipol interaktioner i et givent molekyle.
Hydrogenbånd
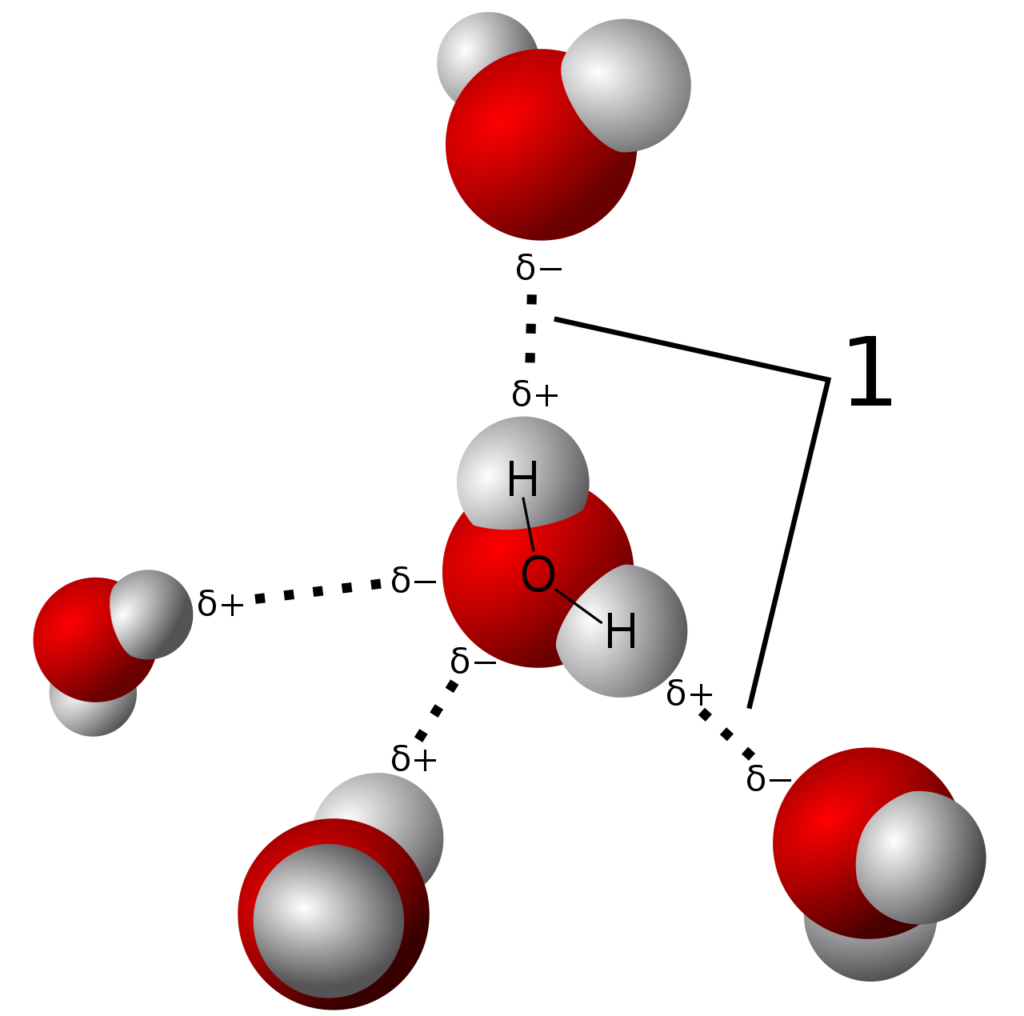
Hydrogenbånd er en type intermolekylær binding, der opstår mellem hydrogenatomer og elektronegativt ladende atomer. Når et hydrogenatom er bundet til et elektronegativt ladet atom, vil elektronerne i hydrogenatomet blive trukket mere mod det elektronegativt ladete atom end mod protonerne i hydrogenatomet. Dette resulterer i en ujævn fordeling af elektronerne i hydrogenatomet, hvilket igen resulterer i en midlertidig polarisering af molekylet.
Når to molekyler med polariserede hydrogenatomer er tæt på hinanden, vil de positive og negative ender tiltrække hinanden, hvilket resulterer i en attraktion mellem molekylerne. Denne attraktion kaldes for hydrogenbånd.
Hydrogenbånd er ikke en permanent binding, men den er stærkere end de svagere intermolekylære bindinger, dispersion forces og dipol-dipol interaktioner. Styrken af hydrogenbånd afhænger af afstanden mellem de polariserede hydrogenatomer, så jo tættere de er på hinanden, jo stærkere vil hydrogenbånden være.
Hydrogenbånd findes i mange molekyler, herunder vand, alkoholer og sukkerarter. Disse molekyler har alle en høj kogepunkt og en høj smeltepunkt, hvilket skyldes de stærke hydrogenbånd. Hydrogenbånd spiller også en vigtig rolle i strukturen af biologiske molekyler som proteiner og DNA.
I termodynamisk sammenhæng kan hydrogenbånd beskrives ved hjælp af entalpi. Når hydrogenbånd brydes, vil dette medføre en entalpifrigørelse, hvilket kan måles ved hjælp et Kalorimeter. Ved at måle entalpifrigørelsen ved hydrogenbåndsbrud kan man beregne styrken af hydrogenbånd i et givent molekyle.
Van der Waals-kræfter
Van der Waals-kræfter er en samlet betegnelse for de intermolekylære bindinger, der er svagere end de stærkere ion-ion interaktioner og hydrogenbånd. Van der Waals-kræfter omfatter dipol-dipol interaktioner, dispersion forces og London-kræfter.
Van der Waals-kræfter omfatter tre forskellige kræfter: dipol-dipol interaktioner, dispersion forces og London-kræfter. Dipol-dipol interaktioner er de elektrostatiske kræfter, der opstår mellem permanente dipoler i molekyler. Dispersion forces er de elektrostatiske kræfter, der opstår mellem alle typer af atomer og molekyler. London-kræfter er de elektrostatiske kræfter, der opstår mellem to nærliggende, neutraliserende atomer eller molekyler.
Van der Waals-kræfter er stærkere end dispersion forces, men stadig relativt svage sammenlignet med andre typer af intermolekylære bindinger. Styrken af Van der Waals-kræfter afhænger af afstanden mellem molekylerne, så jo tættere de er på hinanden, jo stærkere vil Van der Waals-kræfterne være.
Van der Waals-kræfter findes i mange molekyler, herunder nonpolar molekyler og parfumer. Disse molekyler har en lavere kogepunkt og smeltepunkt end polar molekyler på grund af de svage Van der Waals-kræfter. Van der Waals-kræfter spiller også en vigtig rolle i strukturen af mange materialer, herunder plast og metal.
I termodynamisk sammenhæng kan Van der Waals-kræfter beskrives ved hjælp af entalpi. Når Van der Waals-kræfter brydes, vil dette medføre en entalpifrigørelse, hvilket kan måles ved hjælp af et kalorimeter. Ved at måle entalpifrigørelsen ved brud på Van der Waals-kræfter kan man beregne styrken af Van der Waals-kræfter i et givent molekyle.
Eksperimentel bestemmelse af intermolekylære bindinger
Der findes mange forskellige måder, hvorpå intermolekylære bindinger kan bestemmes eksperimentelt. Nogle af de mest almindelige metoder til bestemmelse af intermolekylære bindinger inkluderer:
- Kogepunktsbestemmelse: Kogepunktet for en væske eller et fast stof kan bruges til at bestemme styrken af intermolekylære bindinger. Jo stærkere bindingerne er, desto højere vil kogepunktet være.
- Smeltepunktsbestemmelse: Smeltepunktet for et fast stof kan bruges til at bestemme styrken af intermolekylære bindinger. Jo stærkere bindingerne er, desto højere vil smeltepunktet være.
- Damptryksbestemmelse: Damptrykket for en væske eller et fast stof kan bruges til at bestemme styrken af intermolekylære bindinger. Jo stærkere bindingerne er, desto lavere vil damptrykket være.
- Kalorimeter: Ved at måle entalpifrigørelsen ved brud på intermolekylære bindinger kan man bestemme styrken af bindingerne.
- Spektroskopiske metoder: Der findes mange forskellige spektroskopiske metoder, der kan bruges til at bestemme styrken af intermolekylære bindinger, herunder infrared spektroskopi og Raman spektroskopi.
- Krystallografi: Ved at bestemme strukturen af et krystallinsk materiale kan man bestemme styrken af intermolekylære bindingerne i materialet.
- Mekaniske metoder: Der findes mange forskellige mekaniske metoder, der kan bruges til at bestemme styrken af intermolekylære bindinger, herunder tæthedsbestemmelse, hårdhedsbestemmelse og deformationsbestemmelse
Anvendelser af intermolekylære bindinger
Der findes mange forskellige anvendelser af intermolekylære bindinger inden for en række forskellige områder, herunder kemi, materialevidenskab, medicin og biologi. Nogle eksempler på anvendelser af intermolekylære bindinger inkluderer:
- Opløsning af stoffer: Intermolekylære bindinger spiller en vigtig rolle i opløsning af stoffer. Når et stof opløses i en væske, vil de intermolekylære bindinger mellem væskemolekylerne og stofmolekylerne være stærke nok til at holde stofmolekylerne suspenderet i væsken.
- Struktur af materialer: Intermolekylære bindinger spiller også en vigtig rolle i strukturen af mange materialer. For eksempel er styrken af hydrogenbånd i vand en af grundene til, at vand har en høj kogepunkt.
- Kemiske reaktioner: Intermolekylære bindinger spiller en vigtig rolle i mange kemiske reaktioner, da de kan påvirke stabiliteten og reaktiviteten af de involverede molekyler.
- Biologiske processer: Intermolekylære bindinger spiller en vigtig rolle i mange biologiske processer, herunder strukturen af proteiner og DNA, og i transporten af stoffer gennem biologiske membraner.
- Medicin: Intermolekylære bindinger spiller også en vigtig rolle i mange medicinske anvendelser, herunder i designet af lægemidler og i diagnostiske metoder.
Spørgsmål
I denne Q/A sektion vil vi tage et dybere kig på intermolekylære bindinger og besvare nogle af de mest almindelige spørgsmål, der opstår om emnet.
Er ionbindinger intermolekylære bindinger?
Ionbindinger er en type intermolekylær binding, der opstår mellem ioner. Ions bindinger opstår, når to ioner – enten positivt ladet eller negativt ladet – tiltrækker hinanden på grund af deres modsatte elektriske ladninger. Styrken af ionbindinger afhænger af ladningen på ionerne og afstanden mellem dem.
Ionbindinger er stærkere end de svagere intermolekylære bindinger, dispersion forces og dipol-dipol interaktioner, men stadig svagere end de stærkere hydrogenbånd og covalente bindinger. Ionbindinger findes i mange molekyler og materialer, herunder salte og krystallinske materialer. Ionbindinger spiller også en vigtig rolle i mange kemiske reaktioner og biologiske processer.
Hvad er forskellen på ionbinding og kovalent binding?
Der er mange forskelle mellem ionbinding og kovalent binding. Nogle af de vigtigste forskelle inkluderer:
- Ladning: Ionbinding opstår mellem ioner, der har en positiv eller negativ ladning, mens kovalent binding opstår mellem atomer, der deler elektroner for at få stabile elektronkonfigurationer.
- Styrke: Ionbindinger er stærkere end de svagere intermolekylære bindinger, dispersion forces og dipol-dipol interaktioner, men stadig svagere end de stærkere hydrogenbånd og covalente bindinger. Kovalente bindinger er de stærkeste af alle intermolekylære bindinger.
- Elektroner: Ionbinding opstår på grund af tiltrækningen mellem ioner med modsatte ladninger, mens kovalent binding opstår, når atomer deler elektroner.
- Anvendelse: Ionbindinger findes i mange molekyler og materialer, herunder salte og krystallinske materialer. Kovalente bindinger findes i mange molekyler, herunder organiske molekyler og uorganiske molekyler.
- Kemiske egenskaber: Molekyler med ionbindinger har ofte andre kemiske egenskaber end molekyler med kovalente bindinger. For eksempel har molekyler med ionbindinger tendens til at være elektrisk ledende, mens molekyler med kovalente bindinger er elektrisk isolerende.
Er ionbindinger kovalente?
Nej, ionbindinger er ikke kovalente. Kovalent binding er en type intermolekylær binding, der opstår, når atomer deler elektroner for at opnå stabile elektronkonfigurationer. Kovalent binding er den stærkeste af alle intermolekylære bindinger.
Ionbindinger er en anden type intermolekylær binding, der opstår mellem ioner, der har en positiv eller negativ ladning. Ionbindinger er stærkere end de svagere intermolekylære bindinger, dispersion forces og dipol-dipol interaktioner, men stadig svagere end de stærkere hydrogenbånd og covalente bindinger. Ionbindinger findes i mange molekyler og materialer, herunder salte og krystallinske materialer. Ionbindinger spiller også en vigtig rolle i mange kemiske reaktioner og biologiske processer.
Er dipol-dipol bindinger stærke bindinger?
Dipol-dipol bindinger er en type intermolekylær binding, der opstår mellem dipoler – molekyler med en permanent polarisering. Dipol-dipol bindinger opstår, når de positive ender af to dipoler tiltrækker hinanden, mens de negative ender tiltrækker hinanden. Dipol-dipol bindinger er stærkere end de svagere dispersion forces, men stadig svagere end de stærkere hydrogenbånd, ionbindinger og covalente bindinger.
Styrken af dipol-dipol bindinger afhænger af størrelsen af dipolerne og afstanden mellem dem. Dipol-dipol bindinger findes i mange molekyler, herunder polariseret molekyler som vand og sukker. Dipol-dipol bindinger spiller også en vigtig rolle i mange kemiske reaktioner og biologiske processer.
Hvad menes med en dipol?
En dipol er et molekyle med en permanent polarisering, dvs. at der er en del af molekylet, der er positivt ladet, og en anden del, der er negativt ladet.
Dipoler opstår, når elektronerne i et molekyle er ujævnt fordelt, hvilket resulterer i en polarisering af molekylet. Dipoler findes i mange molekyler, herunder polariseret molekyler som vand og sukker.
Konklusion
I denne artikel har vi set på de forskellige typer af intermolekylære bindinger, der findes, herunder hydrogenbånd, ion-dipol interaktioner, Van der Waals-kræfter og london-kræfter. Vi har også set på, hvordan disse bindinger påvirker strukturen og egenskaberne af molekyler og materialer, samt hvordan de kan bestemmes eksperimentelt.
Intermolekylære bindinger spiller en vigtig rolle i mange områder, herunder kemi, materialevidenskab, medicin og biologi. Ved at forstå styrken og egenskaberne af intermolekylære bindinger kan vi designe og udvikle nye materialer og lægemidler, og forbedre vores forståelse af biologiske processer. Derfor er det vigtigt at fortsætte med at undersøge og forstå intermolekylære bindinger.